神经坏死病毒(NNV)是一种世界范围内流行,严重危害多种海水和淡水鱼类的传染性病原。衣壳蛋白(CP)是该病毒唯一具有致病性和抗原性的结构蛋白,然而有关其免疫优势表位或中和功能位点的公开信息仍然极其缺乏。基于前期基础,本研究利用特异性抗石斑鱼NNV(RGNNV)CP的中和单克隆抗体,结合部分重叠的重组截短蛋白以及合成肽库,在CP中鉴定出两个分别位于S-domain和P-domain的最小B细胞表位122GYVAGFL128和227SLYNDSL233。氨基酸定点突变分析表明,Y123、G126、L128和L228、Y229、N230、D231、L233分别是介导表位与相应抗体直接互作的关键氨基酸残基。一系列生物信息学及系统进化分析显示,227SLYNDSL233在所有NNV基因型中几乎完全保守,暴露在病毒粒子表面突起的顶端周围,具有良好的免疫原性;而122GYVAGFL128在RGNNV以外基因型中具有大量抗原漂移,埋藏在病毒粒子壳区与突起连接处的凹槽中,免疫原性较差。体外封闭实验表明,SLYNDSL合成肽可减少GF-1细胞表面RGNNV的附着,进而抑制病毒的复制增殖,而GYVAGFL合成肽则无此封闭效果。综上所述,227SLYNDSL233是一个受体结合位点,相应抗体与之结合可阻断病毒粒子与易感细胞的粘附,进而产生中和效果;而122GYVAGFL128可能是一个稳定病毒粒子构象的脆弱区域,相应抗体与之结合后可破坏病毒的天然结构,进而产生中和效果。研究结果丰富了人们对NNV抗原分布模式和中和分子基础的理解,为推动研发针对NNV的高效抗病毒药物提供了新的靶点。
该项工作于2023年1月12日以题为《Identification of B-Cell Epitopes on Capsid Protein Reveals Two Potential Neutralization Mechanisms in Red-Spotted Grouper Nervous Necrosis Virus》的论文发表在领域顶尖刊物《Journal of Virology》(IF=6.549)。中国海洋大学水产学院邢婧教授和战文斌教授为本文共同通讯作者,2020级博士研究生张志琪为第一完成人。该研究得到国家重点研发计划(2019YFD0900101、2019YFD0900102、2018YFD0900503)、国家自然科学基金(32173005、31730101、31672684、31672685)和山东省自然科学基金(ZR2020KC025)的支持。
文章链接:https://journals.asm.org/doi/10.1128/jvi.01748-22
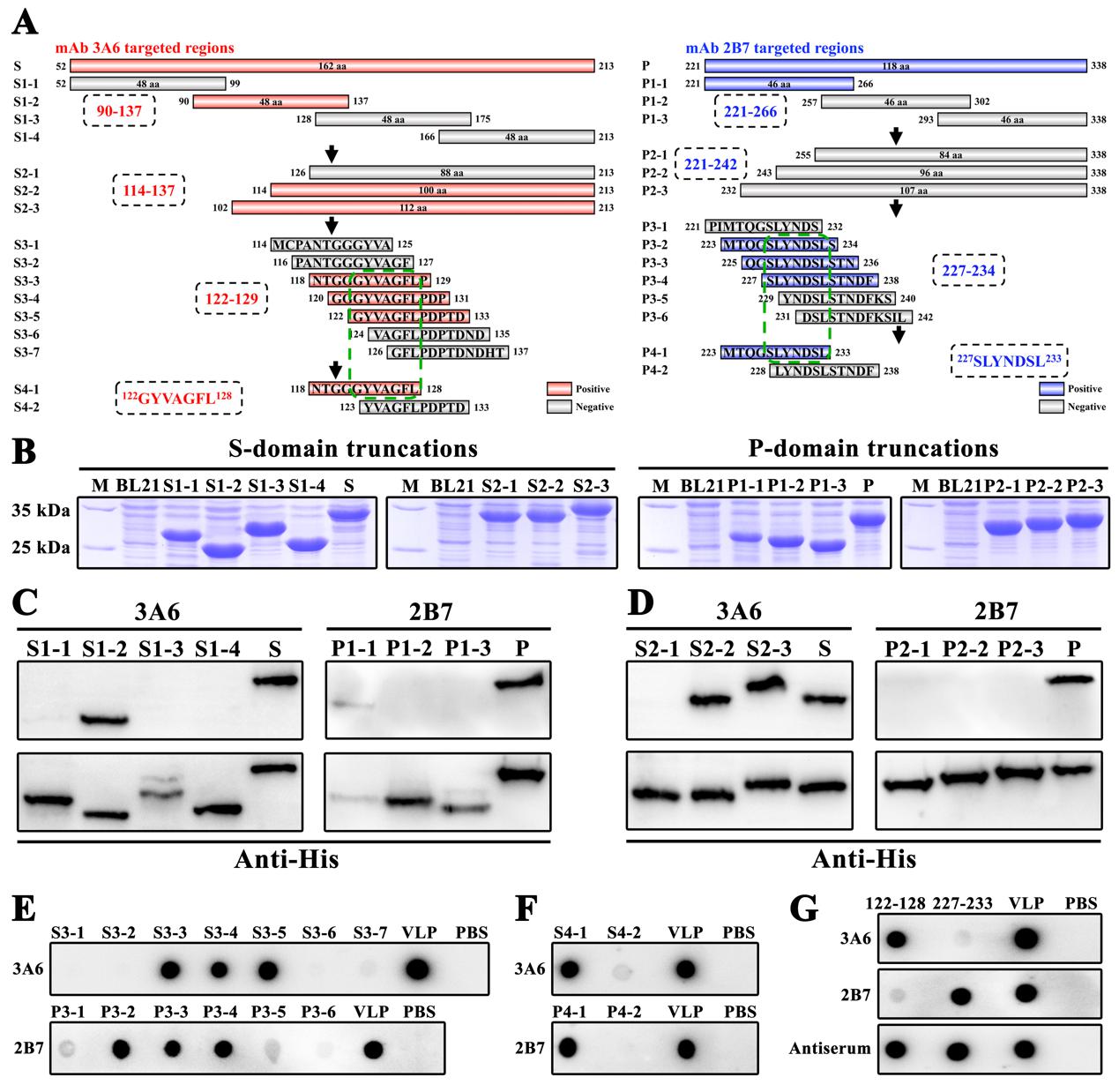
图1 RGNNV CP中B细胞表位的鉴定
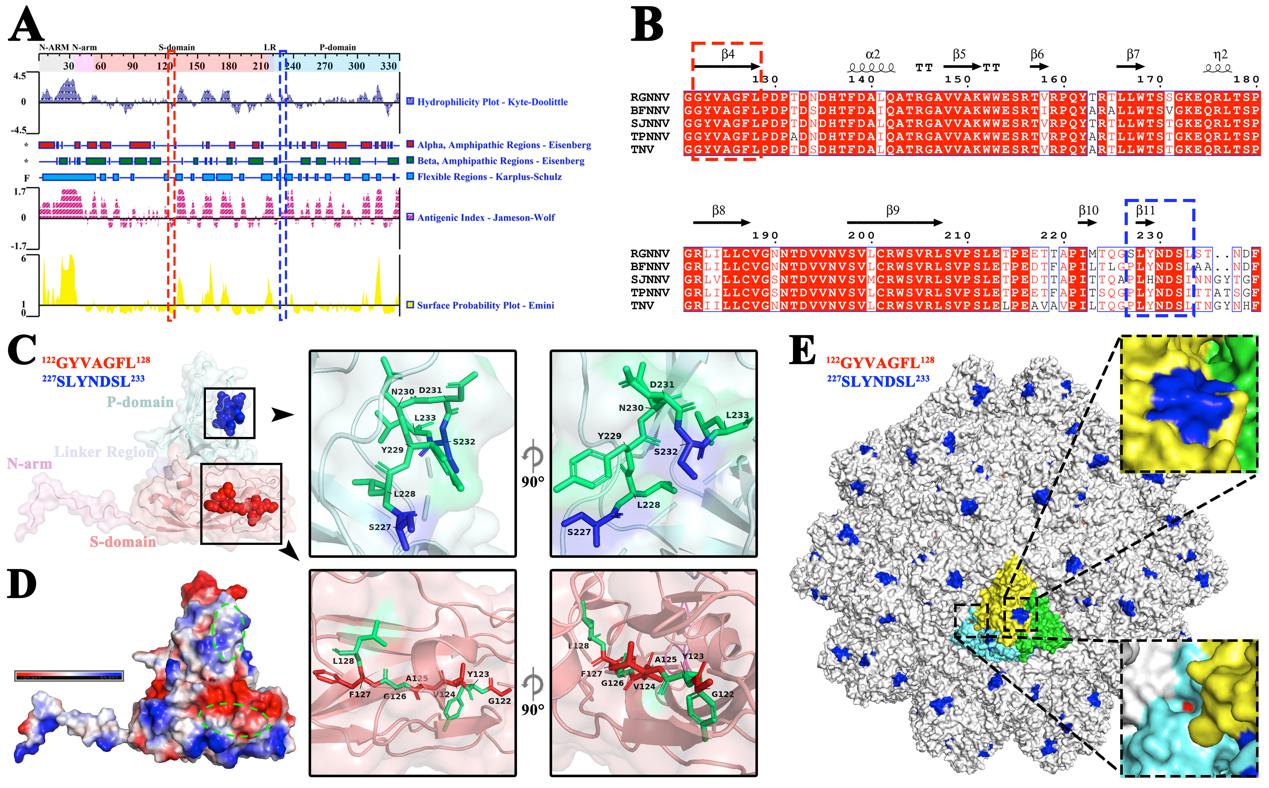
图2 B细胞表位的生物信息学分析

